
Visi iLive saturs ir medicīniski pārskatīts vai pārbaudīts, lai nodrošinātu pēc iespējas lielāku faktisko precizitāti.
Mums ir stingras iegādes vadlīnijas un tikai saikne ar cienījamiem mediju portāliem, akadēmiskām pētniecības iestādēm un, ja vien iespējams, medicīniski salīdzinošiem pārskatiem. Ņemiet vērā, ka iekavās ([1], [2] uc) esošie numuri ir klikšķi uz šīm studijām.
Ja uzskatāt, ka kāds no mūsu saturiem ir neprecīzs, novecojis vai citādi apšaubāms, lūdzu, atlasiet to un nospiediet Ctrl + Enter.
Hipofīzes mikroadenoma: cēloņi, simptomi, draudi, prognoze
Raksta medicīnas eksperts
Pēdējā pārskatīšana: 12.07.2025
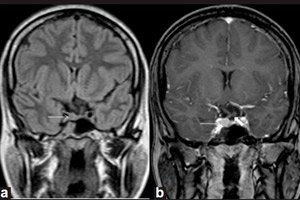
Labdabīgi audzēji, kas rodas endokrīnajos dziedzeros, tiek saukti par adenomām, un hipofīzes mikroadenoma ir neliels tās priekšējās daivas audzējs, kas ražo vairākus svarīgus hormonus.
Epidemioloģija
Hipofīzes audzēju sastopamība tiek lēsta 10–23 % apmērā, un visbiežāk sastopamas ir hipofīzes adenomas (16 %), kurām var būt dažādas formas un izmēri.[ 1 ]
Līdz pat 20–25 % cilvēku var būt nelieli hipofīzes audzēji, mikroadenomas, pat to nezinot, un aptuveni pusē gadījumu šādi audzēji tiek atklāti nejauši smadzeņu attēldiagnostikas laikā.
Prolaktīnu izdalošas mikroadenomu formas veido 45–75% no šādiem audzējiem; AKTH producējošas formācijas veido ne vairāk kā 14% gadījumu, un STH producējošo mikroadenomu biežums nepārsniedz 2%.
Hipofīzes mikroadenoma bērniem un pusaudžiem tiek atklāta 10,7–28 % gadījumu, un vismaz pusei no tiem ir hormonāla neaktivitāte. [ 2 ]
Cēloņi hipofīzes mikroadenomas
Eksperti nezina precīzus mikroadenomas parādīšanās iemeslus hipofīzē, kas ir endokrīnā dziedzeris smadzenēs, kura šūnas ražo:
- kortikotropīns vai AKTH – adrenokortikotropais hormons, kas izraisa steroīdo hormonu sekrēciju virsnieru garozā;
- augšanas hormons STH – somatotropiskais hormons;
- gonadotropīni FSH – folikulus stimulējošais hormons un LH – luteinizējošais hormons, kas nosaka sieviešu dzimumhormonu ražošanu olnīcās un vīriešu dzimumhormonu ražošanu sēkliniekos;
- laktogēnais hormons prolaktīns (PRL);
- tireotropīns jeb vairogdziedzeri stimulējošais hormons (TSH), kas stimulē hormonu sintēzi vairogdziedzerī.
Tiek uzskatīts, ka šo audzēju attīstību var izraisīt traumatiska smadzeņu trauma; nepietiekama asins piegāde hipofīzei; smadzeņu infekcijas vai toksīnu iedarbība (izraisot tūsku un intrakraniālu hipertensiju).
Riska faktori
Ir zināms, ka hipofīzes adenomas un mikroadenomas biežāk rodas, ja ģimenes anamnēzē ir MEN 1 sindroms — multipla endokrīnā adenomatoze 1. tips, kas ir iedzimta. Tādējādi pastāv ģenētiski noteikti riska faktori, kas saistīti ar noteiktām izmaiņām DNS. [ 3 ]
4. tipa multipla endokrīnā neoplāzija (MEN4): MEN 4. tipa neoplāzijai ir mutācija ciklīnatkarīgā kināzes inhibitora 1B (CDKN1B) gēnā, ko raksturo hipofīzes audzēji, hiperparatireoīdisms, sēklinieku un dzemdes kakla neiroendokrīnie audzēji.[ 4 ]
Kārnija komplekss (CNC): Kārnija kompleksā audzēja nomācošajā gēnā PRKAR1A ir germinālās līnijas mutācija, kas izraisa primāru pigmentētu mezglainu virsnieru garozas slimību (PPNAD), sēklinieku audzējus, vairogdziedzera mezgliņus, plankumainu ādas hiperpigmentāciju un akromegāliju.[ 5 ]
Ģimenes izolētu hipofīzes adenomu (FIPA) klīnisko formu raksturo ģenētiski defekti arilhidrogēnskābes receptoru mijiedarbības proteīna (AIP) gēnā, kas ir sastopami aptuveni 15% no visām radniecīgajām un 50% no homogēnajām somatotropīnu ģimenēm.[ 6 ]
Ģimenes izolētas hipofīzes adenomas (FIPA): aptuveni 15% no visiem FIPA gadījumiem pusaudža gados vai agrā pieaugušā vecumā tiek atklāta mutācija arilogļūdeņraža receptoru mijiedarbības proteīnā (AIP). Šie audzēji parasti ir agresīvi un visbiežāk izdala augšanas hormonu, izraisot akromegāliju.[ 7 ]
Nav izslēgta iespēja, ka šāda veida audzējs rodas citu endokrīno dziedzeru un smadzeņu struktūru funkcionālo traucējumu rezultātā, jo īpaši hipotalāma asinsvadu sistēmas izmaiņu rezultātā, kas neiroendokrīnās hipotalāma-hipofīzes sistēmas ietvaros regulē hipofīzes un tās priekšējās daivas - adenohipofīzes - darbību ar tās atbrīvojošajiem hormoniem.
Pathogenesis
Saskaņā ar histoloģiju hipofīzes adenoma ir labdabīgs audzējs; atkarībā no lieluma šie audzēji tiek iedalīti mikroadenomās (līdz 10 mm platākajā vietā), makroadenomās (10–40 mm) un milzu adenomās (40 mm vai vairāk).
Pētot audzēja veidošanās patogenēzi hipofīzē, vēl nav bijis iespējams noteikt tās priekšējās daivas šūnu hiperplastiskās transformācijas mehānismus audzējā.
Eksperti uzskata, ka viena no vispārliecinošākajām versijām ir saistība ar neirotransmitera un hormona dopamīna (kas ir galvenais prolaktīna sekrēcijas inhibitors) metabolisma deregulāciju un/vai hipofīzes šūnu transmembrānu dopamīna receptoru, kas izdala PRL (laktotrofus), funkciju traucējumiem.
Lielākā daļa hipofīzes mikroadenomu ir sporādiskas, bet dažas rodas kā daļa no ģenētiski noteiktiem neiroendokrīniem sindromiem, piemēram, MEN 1, McCune-Albright sindroma, Werner sindroma un Carney sindroma (vai Carney kompleksa). Pēdējais ir saistīts ar paaugstinātu labdabīgu audzēju attīstības risku hormonālajos (endokrīnajos) dziedzeros, tostarp hipofīzē, virsnieru dziedzeros, vairogdziedzerī, olnīcās un sēkliniekos.
Simptomi hipofīzes mikroadenomas
Hipofīzes mikroadenoma var ilgstoši neizrādīt nekādus simptomus. Simptomi atšķiras atkarībā no atrašanās vietas un parasti rodas endokrīnās disfunkcijas rezultātā. Šī ir visbiežāk sastopamā pazīme hormonālas nelīdzsvarotības gadījumos, kas saistīti ar viena vai vairāku hormonu pārmērīgu ražošanu. Vairumā gadījumu pēc atrašanās vietas tā ir hipofīzes priekšējās daļas mikroadenoma.
Pastāv dažādi hipofīzes mikroadenomu veidi, pamatojoties uz to hormonālo aktivitāti. Tādējādi visizplatītākais veids tiek uzskatīts par nefunkcionējošu adenomu – hormonāli neaktīvu hipofīzes mikroadenomu, kas, līdz tā sasniedz noteiktu izmēru, nedod nekādus simptomus. Taču augoša hormonāli neaktīva hipofīzes mikroadenomu var saspiest tuvumā esošās smadzeņu struktūras vai galvaskausa nervus, tāpēc hipofīzes mikroadenoma var kombinēties ar galvassāpēm frontālajā un deniņu rajonā [ 8 ], un ir iespējamas arī redzes problēmas [ 9 ]. Tomēr, kā apgalvo pētnieki, nefunkcionējoši (hormonāli neaktīvi) hipofīzes audzēji 96,5% gadījumu ir makroadenomas. [ 10 ]
Var rasties arī hormonāli aktīva hipofīzes (tās priekšējās daivas) mikroadenoma ar palielinātu hormona prolaktīna sekrēciju - hipofīzes prolaktinoma. Paaugstināta PRL ražošana adenohipofīzes laktotropiskajās šūnās tiek definēta kā hiperprolaktinēmija hipofīzes mikroadenomā.
Kā šāda hipofīzes mikroadenoma izpaužas sievietēm? Patoloģiski augsts šī hormona līmenis kavē estrogēnu veidošanos, un pirmās pazīmes izpaužas menstruālā cikla traucējumos - ar menstruāciju neesamību (amenoreja) un/vai to ovulācijas fāzi. Rezultātā attīstās pastāvīgs galaktorejas-amenorejas sindroms un tiek zaudēta spēja ieņemt bērnu un palikt stāvoklī.
Prolaktīnu izdaloša hipofīzes mikroadenoma vīriešiem var izraisīt hiperprolaktinēmisku hipogonādismu ar samazinātu libido, erektilo disfunkciju, palielinātu krūšu dziedzeru (ginekomastiju) un samazinātu sejas un ķermeņa apmatojumu.
Aktīva mikroadema, kas izdala kortikotropīnu (AKTH), noved pie virsnieru garozas ražoto steroīdo hormonu (glikokortikoīdu) pārpalikuma, kas var izraisīt hipofīzes etioloģijas Itsenko-Kušinga slimību.
Bērniem šāda mikroadenoma var izpausties ar hiperkorticisma (Kušinga sindroma) simptomiem, tostarp galvassāpēm, vispārēju vājumu, pārmērīgu taukaudu nogulsnēšanos uz rumpja, samazinātu kaulu minerālo blīvumu un muskuļu spēku, ādas sloksnveida atrofiju (violetu striju veidā) utt.
Ar aktīvu somatotropīnu producējošu mikroadenomu organismā paaugstinās STH līmenis. Bērnībā tā pārmērīgā anaboliskā iedarbība stimulē gandrīz visu ķermeņa kaulu augšanu un var izraisīt gigantismu; pieaugušajiem akromegālija var attīstīties ar pastiprinātu sejas kaulu augšanu (izraisot izskata deformāciju) un ekstremitāšu locītavu skrimšļu augšanu (kas noved pie to proporciju pārkāpuma un pirkstu sabiezēšanas), ar locītavu sāpēm, pastiprinātu svīšanu un sebuma sekrēciju, kā arī glikozes tolerances traucējumiem.
Ļoti reti (1–1,5 % gadījumu) ir hipofīzes mikroadenoma, kas ražo tireotropīnu, un, tā kā šim hormonam ir stimulējoša iedarbība uz vairogdziedzeri, pacientiem ir hipofīzes hipertireozes klīniskās pazīmes sinusa tahikardijas un sirds priekškambaru fibrilācijas veidā, paaugstināts asinsspiediens, samazināts ķermeņa svars (ar palielinātu apetīti), kā arī paaugstināta nervu uzbudināmība un aizkaitināmība.
Tā sauktā hipofīzes intrasellārā mikroadenoma, sinonīms - hipofīzes endosellārā mikroadenoma, tāpat kā visa hipofīze, atrodas turka sēklā - anatomiski seglveida iedobumā galvaskausa pamatnes sfenoidālajā kaulā. Tajā pašā laikā hipofīze atrodas šīs iedobes apakšā - hipofīzes bedrītē (intrasellārajā reģionā). Un visa atšķirība terminoloģijā ir tāda, ka "iekšpusē" latīņu valodā ir intra, bet grieķu valodā - endom.
Bet hipofīzes mikroadenoma ar suprasellāru augšanu nozīmē, ka audzējs aug uz augšu no hipofīzes bedrītes apakšas.
Hipofīzes cistiskā mikroadenoma ir slēgta maisiņveida struktūra un ir asimptomātiska veidošanās.
Hipofīzes mikroadenoma ar asiņošanu var būt apopleksijas vai hemorāģiska infarkta rezultāts, kas saistīts ar dziedzera palielināšanos un tās priekšējās daivas parenhīmas sinusoidālo kapilāru, neirohemālo sinapšu un/vai portālo asinsvadu bojājumiem.
Hipofīzes mikroadenoma un grūtniecība
Kā jau minēts, sievietes ar prolaktīnu producējošu hipofīzes mikroadenomu parasti ir neauglīgas estrogēna deficīta un GnRH (gonadotropīnu atbrīvojošā hormona) pulsējošas sekrēcijas nomākšanas dēļ. Lai ieņemtu bērnu, prolaktīna līmenis ir jānormalizē, pretējā gadījumā apaugļošanās nenotiek vai grūtniecība tiek pārtraukta pašā sākumā.
- Vai ir iespējams dzemdēt ar hipofīzes mikroadenomu?
Sievietēm ar klīniski funkcionējošām mikroadenomām, kuras ārstē ar dopamīna agonistiem (kabergolīnu vai Dostinex), prolaktīna līmenis var normalizēties un atjaunoties menstruālie cikli un auglība.
Vai ir iespējams barot bērnu ar krūti ar hipofīzes mikroadenomu?
Pēcdzemdību periodā zīdīšana ir atļauta, ja nav audzēja simptomu, taču ir nepieciešams uzraudzīt tā lielumu( izmantojot smadzeņu magnētiskās rezonanses attēlveidošanu).Un, ja audzējs aug, zīdīšana tiek pārtraukta.
- Hipofīzes mikroadenoma un IVF
IVF procedūrai nepieciešama hiperprolaktinēmijas ārstēšana, un procedūru var uzsākt, ja normāls prolaktīna līmenis ir bijis stabils 12 mēnešus un citu hipofīzes hormonu seruma līmeņos nav noviržu.
Komplikācijas un sekas
Kas ir bīstams hipofīzes mikroadenomā? Lai gan šis audzējs ir labdabīgs, tā klātbūtne var izraisīt komplikācijas un sekas, jo īpaši:
- izraisīt hipotalāma-hipofīzes-virsnieru sistēmas disfunkciju ar Itsenko-Kušinga slimības attīstību;
- traucēt menstruālā cikla hormonālo regulāciju sievietēm un izraisīt erektilās disfunkcijas rašanos vīriešiem;
- izraisīt augšanas aizkavēšanos un hipofīzes pundurismu (hipopituitarismu) bērniem;
- provocēt osteoporozes attīstību.
Kad augošs audzējs saspiež redzes nerva šķiedras to krustošanās vietā (kas 80% cilvēku atrodas tieši virs hipofīzes), rodas acu kustīguma traucējumi (oftalmoplēģija) un pakāpeniska perifērās redzes pasliktināšanās. Lai gan mikroadenomas parasti ir pārāk mazas, lai radītu šādu spiedienu.
Vai hipofīzes mikroadenoma var sadzīt? Tā nevar sadzīt, bet laika gaitā hormonāli neaktīvs audzējs bērniem var ievērojami samazināties. Taču aptuveni 10% pacientu mikroadenomas var palielināties.
Diagnostika hipofīzes mikroadenomas
Lai diagnosticētu hipofīzes mikroadenomu, nepieciešama pilnīga pacienta anamnēze un laboratoriskie izmeklējumi: asins analīzes hormonu līmeņa noteikšanai (ko ražo hipofīze), tostarp asins seruma radioimunoanalīze prolaktīna līmeņa noteikšanai.
Ja prolaktīns ir normāls ar hipofīzes mikroadenomu, tad šis audzējs ir hormonāli neaktīvs. Bet, ja ir prolaktinomas simptomi, tad šāds viltus negatīvs rezultāts var būt vai nu laboratorijas testa kļūdas rezultāts, vai arī pacientam ir attīstījusies makroadenoma, kas saspiež hipofīzes kātu.
Turklāt var būt nepieciešami papildu testi, piemēram, vairogdziedzera hormonu (T3 un T4), imūnglobulīnu, interleikīna-6 līmeņa noteikšanai asins serumā.
Mikroadenomu var atklāt tikai ar instrumentālu diagnostiku, izmantojot smadzeņu magnētiskās rezonanses attēlveidošanu (MRI). Mikroadenomu MRI tiek uzskatīta par vizualizācijas standartu, un MRI jutība ar kontrasta pastiprinājumu ir 90%.
MRI hipofīzes mikroadenomas pazīmes ir: dziedzera tilpums mikroadenomas pusē; turkainās sienas izmēra palielināšanās; tās dibena (apakšējās sienas) retināšana un kontūras izmaiņas; hipofīzes infundibula laterālā novirze; noapaļotā apgabala izointensitāte salīdzinājumā ar pelēko vielu T1 un T2 svērtajos attēlos; neliela hiperintensitāte T2 svērtajos attēlos. [ 11 ]
Diferenciālā diagnoze
Diferenciāldiagnostika tiek veikta ar kraniofaringiomu, hipofīzes granulāro šūnu audzēju (horistomu), Ratkes maisiņa cistu, dermoīdu veidošanos, hipofīzes iekaisumu - autoimūnu vai limfocītu hipofizītu, feohromocitomu, vairogdziedzera slimībām utt.
Sievietēm ar anovulācijas ciklu hipofīzes mikroadenoma un policistisko olnīcu sindroms tiek diferencēti, jo 75–90% ovulācijas trūkuma gadījumu ir policistisko olnīcu sindroma sekas.
Kurš sazināties?
Profilakse
Tā kā hipofīzes audzēju vides vai dzīvesveida cēloņi nav zināmi, vienkārši nav iespējams novērst hipofīzes mikroadenomu attīstību.
Prognoze
Lielākā daļa hipofīzes audzēju ir izārstējami. Ja hormonāli aktīva hipofīzes mikroadenomu diagnosticē laikus, atveseļošanās iespējas ir augstas un prognoze ir labvēlīga.
Invaliditāte un hipofīzes mikroadenoma: invaliditāte var būt saistīta ar audzēja augšanu un redzes nerva bojājumiem, kā arī citām šīs patoloģijas sekām, kuru smagums ir individuāls. Un pacienta atzīšana par invalīdu ir atkarīga no esošajām veselības problēmām un funkcionālo traucējumu līmeņa, kam jāatbilst likumdošanā apstiprinātiem kritērijiem.
Hipofīzes mikroadenoma un armija: pacientiem ar šo audzēju (pat ja tas tiek veiksmīgi izņemts) nevajadzētu pārkarst, ilgstoši uzturēties saulē un fiziski pārpūlēties. Tātad, viņi nav piemēroti militārajam dienestam.
Cik ilgi cilvēki dzīvo ar hipofīzes mikroadenomu? Šis audzējs nav vēzis, tāpēc nav paredzamā dzīves ilguma ierobežojumu. Lai gan ar aktīvu STH producējošu mikroadenomu pacientiem var attīstīties hipertensija un palielināties sirds izmērs, un tas var ievērojami samazināt viņu paredzamo dzīves ilgumu. Paaugstināts nāves risks pacientiem, kas vecāki par 45 gadiem, ir novērots ar Itsenko-Kušinga slimību un akromegāliju.

