
Visi iLive saturs ir medicīniski pārskatīts vai pārbaudīts, lai nodrošinātu pēc iespējas lielāku faktisko precizitāti.
Mums ir stingras iegādes vadlīnijas un tikai saikne ar cienījamiem mediju portāliem, akadēmiskām pētniecības iestādēm un, ja vien iespējams, medicīniski salīdzinošiem pārskatiem. Ņemiet vērā, ka iekavās ([1], [2] uc) esošie numuri ir klikšķi uz šīm studijām.
Ja uzskatāt, ka kāds no mūsu saturiem ir neprecīzs, novecojis vai citādi apšaubāms, lūdzu, atlasiet to un nospiediet Ctrl + Enter.
Zinātnieki atklāj jaunu imūnsupresijas mehānismu smadzeņu vēža gadījumā
Pēdējā pārskatīšana: 02.07.2025
Asociētais profesors Filippo Veglia, Ph.D., un viņa komanda Wistar institūtā ir atklājuši galveno mehānismu, ar kuru glioblastoma – nopietns un bieži vien letāls smadzeņu vēzis – nomāc imūnsistēmu, lai audzējs varētu augt neapturami organisma aizsargspējas.
Viņu atklājums tika publicēts rakstā "Glikozes izraisīta histonu laktilēšana veicina monocītu izcelsmes makrofāgu imūnsupresīvo aktivitāti glioblastomā" žurnālā "Immunity".
"Mūsu pētījums liecina, ka vēža pašvairošanās mehānismi, ja tie tiek pietiekami izprasti, var tikt ļoti efektīvi izmantoti cīņā pret slimību," sacīja Dr. Veglia.
"Es ceru uz turpmākiem pētījumiem par vielmaiņas mediētiem imūnsupresijas mehānismiem glioblastomā un ceru, ka mēs turpināsim uzzināt vairāk par to, kā labāk izprast un cīnīties pret šo vēzi."
Līdz šim ir maz pētīts, kā monocītu izcelsmes makrofāgi un mikroglijas glioblastomā rada imūnsupresīvu audzēja mikrovidi.
Veglia laboratorija pētīja glioblastomas imūnsupresijas šūnu mehānismus un atklāja, ka glioblastomas progresēšanas laikā monocītu izcelsmes makrofāgu skaits sāk pārsniegt mikrogliju, kas liecina, ka monocītu izcelsmes makrofāgu pārsvars audzēja mikrovidē ir labvēlīgs vēzim imūnsistēmas apiešanas ziņā.
Patiešām, monocītu izcelsmes makrofāgi, bet ne mikroglija, bloķēja T šūnu (imūnšūnu, kas iznīcina audzēja šūnas) aktivitāti preklīniskajos modeļos un pacientiem. Komanda to apstiprināja, izvērtējot preklīniskos glioblastomas modeļus ar mākslīgi samazinātu monocītu izcelsmes makrofāgu skaitu.
Kā paredzēts, modeļi ar mazāk ļaundabīgiem makrofāgiem audzēja mikrovidē uzrādīja labākus rezultātus salīdzinājumā ar standarta glioblastomas modeļiem.
Glioblastoma veido nedaudz vairāk par pusi no visiem ļaundabīgajiem audzējiem, kas rodas smadzenēs, un pacientu, kuriem diagnosticēta šī slimība, prognoze ir ārkārtīgi slikta: tikai 25% pacientu izdzīvo pirmo gadu pēc diagnozes noteikšanas. Glioblastoma ir bīstama ne tikai tās atrašanās vietas dēļ smadzenēs, bet arī imūnsupresīvās audzēja mikrovides dēļ, kas padara glioblastomu rezistentu pret daudzsološām imunoterapijām.
Programmējot noteiktas imūnās šūnas, piemēram, makrofāgus (no monocītu iegūtos makrofāgus un mikrogliju), lai tie darbotos audzēja labā, nevis pret to, glioblastoma rada sev audzēja mikrovidi, kas ļauj vēzim agresīvi augt, vienlaikus izvairoties no pretvēža imūnās atbildes.
Mehānisma precizējums
Apstiprinājusi monocītu izcelsmes makrofāgu lomu, Weglia laboratorija centās precīzi saprast, kā šīs ar vēzi saistītās imūnās šūnas darbojas pret imūnsistēmu.
Viņi sekvencēja makrofāgus, lai noteiktu, vai šūnām ir kādi patoloģiski gēnu ekspresijas modeļi, kas varētu liecināt par gēniem, kuriem ir nozīme imūnsupresijā, un viņi arī pārbaudīja makrofāgu vielmaiņas modeļus, lai noskaidrotu, vai patoloģiskā gēnu ekspresija ir saistīta ar vielmaiņu.
Gēnu un vielmaiņas analīze viņus noveda pie glikozes metabolisma. Virkne testu parādīja, ka no monocītu atvasināti makrofāgi ar paaugstinātu glikozes metabolismu un GLUT1, galvenā glikozes transportētāja, ekspresiju bloķēja T šūnu darbību, atbrīvojot interleikīnu-10 (IL-10).
Komanda pierādīja, ka glioblastoma traucē glikozes metabolismu šajos makrofāgos, izraisot to imūnsupresīvo aktivitāti.
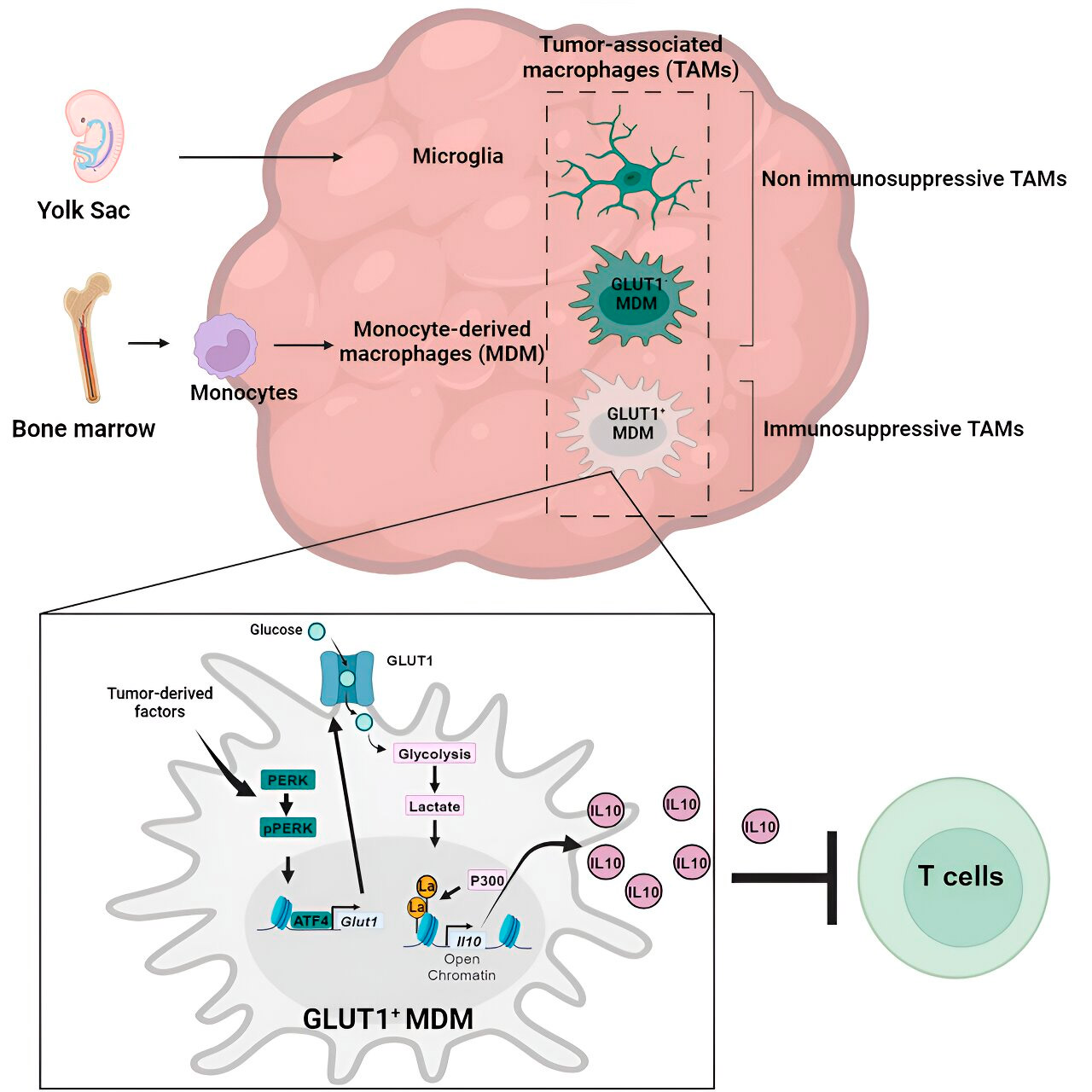
Histonu laktilēšana un tās loma
Pētnieki atklāja, ka monocītu izcelsmes makrofāgu glikozes metabolisma izraisītās imūnsupresīvās aktivitātes atslēga ir process, ko sauc par "histonu laktāciju". Histoni ir strukturāli proteīni genomā, kuriem noteiktos kontekstos ir galvenā loma tādu gēnu kā IL-10 ekspresijā.
Ātri metabolizējot glikozi, monocītu atvasinātie makrofāgi ražo laktātu, kas ir glikozes metabolisma blakusprodukts. Histoni var tikt "laktilēti" (t. i., laktāts tiek integrēts histonos) tādā veidā, ka histonu organizācija veicina IL-10 ekspresiju, ko monocītu atvasinātie makrofāgi ražo, lai atbalstītu vēža šūnu augšanu.
Problēmas risinājums
Bet kā var apturēt monocītu izcelsmes makrofāgu imūnsupresīvo aktivitāti, kas saistīta ar glikozes metabolismu? Dr. Veglia un viņa komanda atrada iespējamu risinājumu: PERK, enzīmu, ko viņi identificēja kā glikozes metabolisma un GLUT1 ekspresijas regulatoru makrofāgos.
Glioblastomas preklīniskajos modeļos, mērķējot uz PERK, tika traucēta histonu laktilācija un makrofāgu imūnsupresīvā aktivitāte, un, kombinējot ar imunoterapiju, tika bloķēta glioblastomas progresēšana un inducēta ilgstoša imunitāte, kas aizsargāja smadzenes no audzēja ataugšanas, kas liecina, ka PERK-histonu laktilācijas ass mērķēšana varētu būt dzīvotspējīga stratēģija cīņai pret šo nāvējošo smadzeņu vēzi.
