
Visi iLive saturs ir medicīniski pārskatīts vai pārbaudīts, lai nodrošinātu pēc iespējas lielāku faktisko precizitāti.
Mums ir stingras iegādes vadlīnijas un tikai saikne ar cienījamiem mediju portāliem, akadēmiskām pētniecības iestādēm un, ja vien iespējams, medicīniski salīdzinošiem pārskatiem. Ņemiet vērā, ka iekavās ([1], [2] uc) esošie numuri ir klikšķi uz šīm studijām.
Ja uzskatāt, ka kāds no mūsu saturiem ir neprecīzs, novecojis vai citādi apšaubāms, lūdzu, atlasiet to un nospiediet Ctrl + Enter.
Vairogdziedzera dziedzeri
Raksta medicīnas eksperts
Pēdējā pārskatīšana: 04.07.2025

1879. gadā zviedru zinātnieks S. Sandstrēms aprakstīja cilvēka epitēlijķermenīšus un deva tiem nosaukumu. Epitēlijķermenīši ir dzīvībai svarīgi orgāni. To funkcija ir producēt un izdalīt epitēlijķermenīšu hormonu (PTH), kas ir viens no galvenajiem kalcija un fosfora metabolisma regulatoriem.
Pāra augšējais epitēlijķermenītis (glandula parathyroidea superior) un apakšējais epitēlijķermenītis (glandula parathyroidea inferior) ir apaļi vai olveida ķermeņi, kas atrodas uz katras vairogdziedzera daivas aizmugurējās virsmas: viens dziedzeris augšpusē, otrs apakšā. Katra dziedzera garums ir 4-8 mm, platums 3-4 mm, biezums 2-3 mm. Šo dziedzeru skaits nav nemainīgs un var mainīties no 2 līdz 7-8, vidēji to ir četri. Dziedzeru kopējā masa ir vidēji 1,18 g.
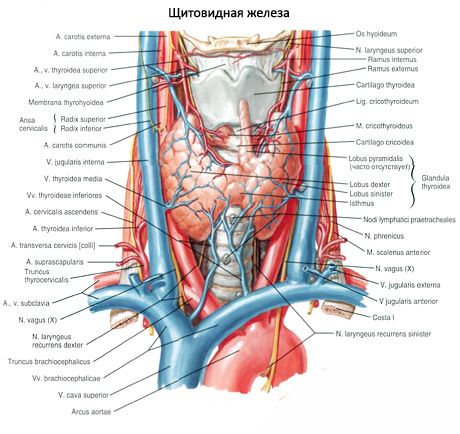
Epitēlijķermenīši atšķiras no vairogdziedzera ar savu gaišāko krāsu (bērniem tie ir gaiši rozā, pieaugušajiem - dzeltenbrūni). Bieži epitēlijķermenīši atrodas vietā, kur vairogdziedzera audus iekļūšanas vietā iekļūst apakšējās vairogdziedzera artērijas vai to zari. Epitēlijķermenīšus no apkārtējiem audiem atdala to pašu šķiedrainā kapsula, no kuras saistaudu slāņi stiepjas dziedzeros. Pēdējie satur lielu skaitu asinsvadu un sadala epitēlijķermenīšus epitēlija šūnu grupās.
Dziedzeru parenhīmu veido galvenie un acidofīlie paratirocīti, kas veido auklas un kopas, ko ieskauj plāni saistaudu šķiedru kūlīši. Abi šūnu veidi tiek uzskatīti par dažādām paratirocītu attīstības stadijām. Galvenajiem paratirocītiem ir daudzstūra forma, bazofīla citoplazma ar lielu ribosomu skaitu. Starp šīm šūnām izšķir tumšās (aktīvi sekretējošās) un gaišās (mazāk aktīvās). Acidofīlie paratirocīti ir lieli, ar skaidrām kontūrām, satur daudz mazu mitohondriju ar glikogēna daļiņām.
Epitēlijķermenīšu hormons paratiroksīns (parathormons) ir olbaltumvielu sastāvs un ir iesaistīts fosfora-kalcija metabolisma regulēšanā. Parathormons samazina kalcija izdalīšanos ar urīnu un palielina tā uzsūkšanos zarnās D vitamīna klātbūtnē. Tireokalcitonīns ir parathormona antagonists.
Parathormonu embrioģenēze
Epitēlijķermenīši attīstās no pārī savienoto III un IV žaunu kabatu epitēlija. 7. attīstības nedēļā ķermeņu epitēlija rudimenti atdalās no žaunu kabatu sienām un augšanas procesā pārvietojas astes virzienā. Pēc tam veidojošie epitēlijķermenīši ieņem tiem pastāvīgu vietu vairogdziedzera labās un kreisās daivas aizmugurējās virsmās.
 [ 7 ], [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ]
[ 7 ], [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ]
Parathormonu asinsvadi un nervi
Epitēlijķermenīšu asinsapgādi nodrošina augšējās un apakšējās vairogdziedzera artēriju zari, kā arī barības vada un trahejas zari. Venozās asinis izplūst pa tāda paša nosaukuma vēnām. Epitēlijķermenīšu inervācija ir līdzīga vairogdziedzera inervācijai.
Ar vecumu saistītas epitēlijķermenīšu īpašības
Jaundzimušajam epitēlijķermenīšu kopējā masa svārstās no 6 līdz 9 mg. Pirmajā dzīves gadā to kopējā masa palielinās 3–4 reizes, līdz 5 gadu vecumam tā atkal divkāršojas, bet līdz 10 gadu vecumam trīskāršojas. Pēc 20 gadiem četru epitēlijķermenīšu kopējā masa sasniedz 120–140 mg un saglabājas nemainīga līdz sirmam vecumam. Visos vecumos epitēlijķermenīšu masa sievietēm ir nedaudz lielāka nekā vīriešiem.
Parasti cilvēkam ir divi epitēlijķermenīšu pāri (augšējais un apakšējais), kas atrodas vairogdziedzera aizmugurējā virsmā, ārpus tā kapsulas, netālu no augšējā un apakšējā pola. Tomēr epitēlijķermenīšu skaits un lokalizācija var atšķirties; dažreiz var atrast līdz pat 12 epitēlijķermenīšiem. Tie var atrasties vairogdziedzera un aizkrūtes dziedzeru audos, priekšējā un aizmugurējā mediastīnā, perikardā, aiz barības vada, miega artērijas bifurkācijas rajonā. Augšējiem epitēlijķermenīšiem ir saplacināta olveida forma, apakšējiem - sfēriski. To izmēri ir aptuveni no 6x3 līdz 4x1,5 - 3 mm, kopējais svars ir no 0,05 līdz 0,5 g, krāsa ir sarkanīga vai dzeltenbrūna. Asins piegādi epitēlijķermenīšiem galvenokārt veic apakšējās vairogdziedzera artērijas zari, venozā attece notiek caur vairogdziedzera, barības vada un trahejas vēnām. Epitēlijķermenīšus inervē recidivējošā un augšējā balsenes nerva simpātiskās šķiedras, parasimpātisko inervāciju veic vagusa nervi. Epitēlijķermenīšus klāj plāna saistaudu kapsula; no tās stiepjas starpsienas, kas iekļūst dziedzeros. Tajos ir asinsvadi un nervu šķiedras. Epitēlijķermenīšu parenhīmu veido paratirocīti jeb galvenās šūnas, starp kurām atkarībā no iekrāsošanās pakāpes izšķir hormonāli aktīvas gaišas vai spīdīgas šūnas, kā arī miera stāvokļa tumšas šūnas. Galvenās šūnas veido kopas, auklas un ķekarus, bet gados vecākiem cilvēkiem - folikulus ar koloīdu dobumā. Pieaugušajiem parādās šūnas, kas galvenokārt atrodas epitēlijķermenīšu perifērijā, iekrāsotas ar eozīnu - eozinofilas vai oksifīlas šūnas, kas ir deģenerējošas galvenās šūnas. Epitēlijķermenīšos var atrast arī pārejas formas starp galvenajām un oksifīlajām šūnām.
Pirmie panākumi parathormona sintēzes jautājumu noskaidrošanā, struktūras atšifrēšanā un metabolisma izpētē tika gūti pēc 1972. gada. Parathormons ir vienas ķēdes polipeptīds, kas sastāv no 84 aminoskābju atlikumiem, bez cisteīna, ar molekulmasu aptuveni 9500 daltonu, kas veidojas parathormonos no bioprekursora - proparathormona (proPTH), kuram NH2 galā ir 6 papildu aminoskābes . ProPTH tiek sintezēts parathormonu galvenajās šūnās (to granulārajā endoplazmatiskajā retikulumā) un proteolītiskās šķelšanās procesā Goldži aparātā tiek pārveidots par parathormonu. Tā bioloģiskā aktivitāte ir ievērojami zemāka nekā PTH aktivitāte. Acīmredzot proPTH nav atrodams veselu cilvēku asinīs, bet patoloģiskos apstākļos (ar parathormona adenomu) tas var izdalīties asinīs kopā ar PTH. Nesen tika atklāts proPTH prekursors - preproPTH, kas NH2 galā satur papildu 25 aminoskābju atlikumus. Tādējādi preproPTH satur 115 aminoskābju atlikumus, proPTH - 90 un PTH - 84.
Liellopu un cūku parathormona struktūra tagad ir pilnībā noteikta. Cilvēka parathormons ir izolēts no parathormona adenomām, taču tā struktūra ir atšifrēta tikai daļēji. Parathormona struktūrā pastāv atšķirības, taču dzīvnieku un cilvēku parathormoniem piemīt krusteniska imunoreaktivitāte. Polipeptīds, kas sastāv no pirmajiem 34 aminoskābju atlikumiem, praktiski saglabā dabiskā hormona bioloģisko aktivitāti. Tas ļauj pieņemt, ka atlikušie gandrīz % molekulas karboksilgalā nav tieši saistīti ar parathormona galveno iedarbību. Parathormona fragments 1-29 arī uzrāda noteiktu bioloģisko un imunoloģisko aktivitāti. Bioloģiski neaktīvais fragments 53-84 arī uzrāda imunoloģisku efektu, t.i., šīs parathormona īpašības uzrāda vismaz 2 tā molekulas sekcijas.
Asinīs cirkulējošais parathormons ir heterogēns un atšķiras no dabiskā hormona, ko izdala parathormona dziedzeri. Asinīs izšķir vismaz trīs dažādus parathormona veidus: neskartu parathormonu ar molekulmasu 9500 daltonu; bioloģiski neaktīvas vielas no parathormona molekulas karboksildaļas ar molekulmasu 7000–7500 daltonu; bioloģiski aktīvas vielas ar molekulmasu aptuveni 4000 daltonu.
Vēl mazāki fragmenti tika atrasti venozās asinīs, kas norāda, ka tie veidojušies perifērijā. Galvenie orgāni, kuros veidojās parathormona fragmenti, bija aknas un nieres. Parathormona fragmentācija šajos orgānos bija palielināta aknu patoloģijas un hroniskas nieru mazspējas (HN) gadījumā. Šādos apstākļos parathormona fragmenti asinsritē saglabājās ievērojami ilgāk nekā veseliem indivīdiem. Aknas absorbēja galvenokārt neskartu parathormonu, bet neizvadīja no asinīm ne karboksilterminālos, ne aminoterminālos parathormona fragmentus. Nierēm bija vadošā loma parathormona metabolismā. Tās veidoja gandrīz 60% no karboksilterminālā imunoreaktīvā hormona metabolisma klīrensa un 45% no parathormona aminoterminālā fragmenta. Parathormona aktīvā aminoterminālā fragmenta metabolisma galvenā zona bija kauli.
Tika konstatēta pulsējoša parathormona sekrēcija, visintensīvākā naktī. Pēc 3-4 stundām no nakts miega sākuma tā saturs asinīs ir 2,5-3 reizes lielāks nekā vidējais dienas līmenis.
Parathormona galvenā funkcija ir uzturēt kalcija homeostāzi. Vienlaikus seruma kalcijs (kopējais un īpaši jonizētais) ir galvenais parathormona sekrēcijas regulators (kalcija līmeņa samazināšanās stimulē parathormona sekrēciju, bet paaugstināšanās to nomāc), t.i., regulācija notiek pēc atgriezeniskās saites principa. Hipokalciēmijas apstākļos palielinās proPTH pārvēršanās parathormonā. Svarīga loma parathormona izdalīšanā ir arī magnija saturam asinīs (tā paaugstināts līmenis stimulē, bet pazemināts līmenis nomāc parathormona sekrēciju). Parathormona galvenie mērķi ir nieres un skeleta kauli, taču ir zināma parathormona ietekme uz kalcija uzsūkšanos zarnās, ogļhidrātu toleranci, seruma lipīdu līmeni, tā loma impotences, ādas niezes u.c. attīstībā.
Lai raksturotu parathormona ietekmi uz kauliem, ir jāsniedz īsa informācija par kaulu audu struktūru, to fizioloģiskās rezorbcijas un pārveidošanās iezīmēm.
Ir zināms, ka lielākā daļa kalcija organismā (līdz pat 99%) atrodas kaulu audos. Tā kā tas kaulos ir atrodams fosfora-kalcija savienojumu veidā, arī kaulos ir atrodami % no kopējā fosfora satura. To audi, neskatoties uz šķietamo statisko raksturu, pastāvīgi tiek pārveidoti, aktīvi vaskularizēti un tiem piemīt augstas mehāniskās īpašības. Kauls ir dinamiska fosfora, magnija un citu savienojumu "depo", kas nepieciešami homeostāzes uzturēšanai minerālvielu metabolismā. Tā struktūra ietver blīvus minerālu komponentus, kas ir cieši saistīti ar organisko matricu, kas sastāv no 90-95% kolagēna, neliela daudzuma mukopolisaharīdu un nekolagēna olbaltumvielu. Kaula minerālo daļu veido hidroksiapatīts - tā empīriskā formula ir Ca10 (PO4) 6 (OH) 2 - un amorfs kalcija fosfāts.
Kaulu veido osteoblasti, kas rodas no nediferencētām mezenhīma šūnām. Tās ir mononukleāras šūnas, kas iesaistītas organiskās kaula matricas komponentu sintēzē. Tās atrodas monoslānī uz kaula virsmas un cieši saskaras ar osteoīdu. Osteoblasti ir atbildīgi par osteoīda nogulsnēšanos un tā sekojošo mineralizāciju. To vitālās aktivitātes produkts ir sārmainā fosfatāze, kuras saturs asinīs ir netiešs to aktivitātes rādītājs. Mineralizēta osteoīda ieskauti daži osteoblasti pārvēršas osteocītos - mononukleārās šūnās, kuru citoplazma veido kanālus, kas saistīti ar blakus esošo osteocītu kanāliem. Tie nepiedalās kaulu remodelācijā, bet ir iesaistīti perilakunāras destrukcijas procesā, kas ir svarīgi kalcija līmeņa ātrai regulēšanai asins serumā. Kaulu rezorbciju veic osteoklasti - milzu polinukleāras šūnas, kas acīmredzot veidojas, saplūstot mononukleāriem makrofāgiem. Tiek arī pieņemts, ka osteoklastu prekursori var būt kaulu smadzeņu hematopoētiskās cilmes šūnas. Tās ir kustīgas, veido slāni, kas saskaras ar kaulu, atrodas tā vislielākās rezorbcijas zonās. Proteolītisko enzīmu un skābās fosfatāzes izdalīšanās dēļ osteoklasti izraisa kolagēna degradāciju, hidroksiapatītu destrukciju un minerālvielu izvadīšanu no matrices. Jaunizveidojušies vāji mineralizēti kaula audi (osteoīds) ir izturīgi pret osteoklastu rezorbciju. Osteoblastu un osteoklastu funkcijas ir neatkarīgas, bet koordinētas viena ar otru, kas noved pie normālas skeleta remodelācijas. Kaula augšana garumā ir atkarīga no endohondrālās osifikācijas, platuma un biezuma pieaugums - no periosteālās osifikācijas. Klīniskie pētījumi ar 47 Ca ir parādījuši, ka katru gadu atjaunojas līdz pat 18% no kopējā kalcija satura skeletā. Kad kauli ir bojāti (lūzumi, infekcijas procesi), izmainītais kauls tiek resorbēts un veidojas jauns kauls.
Šūnu kompleksus, kas iesaistīti lokālajā kaulu rezorbcijas un veidošanās procesā, sauc par daudzšūnu remodelācijas pamata vienībām (BMU). Tie regulē kalcija, fosfora un citu jonu lokālo koncentrāciju, kaula organisko komponentu, jo īpaši kolagēna, sintēzi, tā organizāciju un mineralizāciju.
Parathormona galvenā ietekme uz skeleta kauliem ir rezorbcijas procesu pastiprināšana, ietekmējot gan kaulu struktūras minerālos, gan organiskos komponentus. Parathormons veicina osteoklastu augšanu un to aktivitāti, ko pavada pastiprināta osteolītiska iedarbība un kaulu rezorbcijas palielināšanās. Šajā gadījumā hidroksiapatīta kristāli izšķīst, atbrīvojot kalciju un fosforu asinīs. Šis process ir galvenais mehānisms kalcija līmeņa paaugstināšanai asinīs. Tas sastāv no trim komponentiem: kalcija mobilizācijas no perilakunārā kaula (dziļajiem osteocītiem); osteoprogeneratoru šūnu proliferācijas osteoklastos; nemainīga kalcija līmeņa uzturēšana asinīs, regulējot tā izdalīšanos no kaula (virspusējiem osteocītiem).
Tādējādi parathormons sākotnēji palielina osteocītu un osteoklastu aktivitāti, pastiprinot osteolīzi, izraisot kalcija līmeņa paaugstināšanos asinīs un palielinātu kalcija un oksiprolīna izdalīšanos ar urīnu. Šī ir pirmā, kvalitatīvā, ātrā parathormona iedarbība. Otrā parathormona iedarbība uz kauliem ir kvantitatīva. Tā ir saistīta ar osteoklastu kopuma palielināšanos. Ar aktīvu osteolīzi rodas stimuls pastiprinātai osteoblastu proliferācijai, tiek aktivizēta gan rezorbcija, gan kaulu veidošanās ar rezorbcijas pārsvaru. Ar parathormona pārpalikumu rodas negatīvs kaulu līdzsvars. To pavada pārmērīga oksiprolīna - kolagēna degradācijas produkta - un siālskābju, kas iekļautas mukopolisaharīdu struktūrā, izdalīšanās. Parathormons aktivizē ciklisko adenozīna monofosfātu (cAMP). Paaugstināta cAMP izdalīšanās ar urīnu pēc parathormona ievadīšanas var kalpot kā audu jutības pret to indikators.
Parathormona svarīgākā ietekme uz nierēm ir tā spēja samazināt fosfora reabsorbciju, palielinot fosfatūriju. Redukcijas mehānisms dažādās nefrona daļās ir atšķirīgs: proksimālajā daļā šī parathormona ietekme ir saistīta ar palielinātu caurlaidību un notiek, piedaloties cAMP, savukārt distālajā daļā tā nav atkarīga no cAMP. Parathormona fosfaturiskā ietekme mainās līdz ar D vitamīna deficītu, metabolisko acidozi un samazinātu fosfora saturu. Parathormoni nedaudz palielina kopējo kalcija reabsorbciju tubulārajās daļās. Vienlaikus tas to samazina proksimālajās daļās un palielina distālajās daļās. Pēdējam ir dominējoša nozīme - parathormons samazina kalcija klīrensu. Parathormons samazina nātrija un tā bikarbonāta reabsorbciju tubulārajās daļās, kas var izskaidrot acidozes attīstību hiperparatireoīdā. Tas palielina 1,25-dioksiholekalciferola 1,25(OH2)D3 veidošanos nierēs - D3 vitamīna aktīvā forma. Šis savienojums palielina kalcija reabsorbciju tievajās zarnās, stimulējot specifiska kalciju saistoša proteīna (CaBP) aktivitāti tās sienā.
Normāls parathormona līmenis ir vidēji 0,15–0,6 ng/ml. Tas mainās atkarībā no vecuma un dzimuma. Vidējais parathormona saturs asinīs cilvēkiem vecumā no 20 līdz 29 gadiem ir (0,245±0,017) ng/ml, 80–89 gadiem - (0,545±0,048) ng/ml; parathormona līmenis 70 gadus vecām sievietēm ir (0,728±0,051) ng/ml, vīriešiem tajā pašā vecumā - (0,466±0,40) ng/ml. Tādējādi parathormona saturs palielinās līdz ar vecumu, bet lielākā mērā sievietēm.
Parasti hiperkalciēmijas diferenciāldiagnozei jāizmanto vairāki dažādi testi.
Mēs piedāvājam mūsu izstrādāto klīnisko un patogenētisko klasifikāciju, kuras pamatā ir O. V. Nikolajeva un V. N. Tarkajevas (1974) klasifikācija.
Ar parathormona sekrēcijas traucējumiem un jutību pret to saistīto slimību klīniskā un patogenētiskā klasifikācija
Primārais hiperparatireoīdisms
- Pēc patogenēzes:
- hiperfunkcionējoša(-as) adenoma(-as);
- OGD hiperplāzija;
- hiperfunkcionējoša epitēlijķermenīšu karcinoma;
- I tipa vairāku endokrīnās sistēmas neoplāzija ar hiperparatireozi (Vermera sindroms);
- II tipa multipla endokrīnā neoplāzija ar hiperparatireozi (Sipple sindroms).
- Saskaņā ar klīniskajām pazīmēm:
- kaulu forma:
- osteoporotisks,
- fibrocistiskais osteīts,
- "Pagetoīds";
- Visceropātiskā forma:
- ar dominējošiem bojājumiem nierēm, kuņģa-zarnu traktam, neiropsihiatriskajai sfērai;
- jaukta forma.
- kaulu forma:
- Lejup pa straumi:
- pikants;
- hronisks.
Sekundāra hiperparatireoze (paratireoīdu sekundāra hiperfunkcija un hiperplāzija ar ilgstošu hipokalcēmiju un hiperfosfatemiju)
- Nieru patoloģija:
- hroniska nieru mazspēja;
- tubulopātija (Albraita-Fankoni tips);
- nieru rahīts.
- Zarnu patoloģija:
- malabsorbcijas sindroms.
- Kaulu patoloģija:
- senila osteomalācija;
- pēcdzemdību periodā;
- idiopātisks;
- Pageta slimība.
- D vitamīna deficīts:
- nieru slimība;
- aknas;
- iedzimts enzīmu deficīts.
- Ļaundabīgas slimības: mieloma.
Terciārā hiperparatireoze
- Autonomi funkcionējoša(-as) epitēlijķermenīšu adenoma(-as), kas attīstās uz ilgstošas sekundāras hiperparatireozes fona.
Pseidohiperparatireoze
- Parathormona ražošana audzējos, kuru izcelsme nav paratireoīdā dziedzera.
Hormonāli neaktīvi cistiskie un audzēja veidojumi epitēlijķermenīšos
- Cista.
- Hormonāli neaktīvi audzēji vai karcinoma.
Hipoparatireoze
- Iedzimta epitēlijķermenīšu nepietiekama attīstība vai to neesamība.
- Idiopātiska, autoimūna izcelsme.
- Pēcoperācijas periods, attīstīts saistībā ar epitēlijķermenīšu izņemšanu.
- Pēcoperācijas periods asinsrites un inervācijas traucējumu dēļ.
- Radiācijas bojājumi, eksogēni un endogēni (ārējā staru terapija, vairogdziedzera slimību ārstēšana ar radioaktīvo jodu).
- Epitēlijķermenīšu bojājumi asiņošanas vai infarkta dēļ.
- Infekcijas bojājumi.
Pseidohipoparatireoze
- I tips - mērķa orgānu nejutīgums pret parathormonu, atkarīgs no adenilātciklāzes;
- II tips - mērķa orgānu nejutīgums pret parathormonu, neatkarīgi no adenilātciklāzes, iespējams, autoimūnas izcelsmes.
Pseidopseidohipoparatireoze
Pseidohipoparatireoīdisma somatisko pazīmju klātbūtne veseliem radiniekiem pacientu ar pseidohipoparatireozi ģimenēs bez raksturīgiem bioķīmiskiem traucējumiem un bez tetānijas.
 [ 13 ], [ 14 ], [ 15 ], [ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ], [ 21 ]
[ 13 ], [ 14 ], [ 15 ], [ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ], [ 21 ]
Использованная литература

