
Visi iLive saturs ir medicīniski pārskatīts vai pārbaudīts, lai nodrošinātu pēc iespējas lielāku faktisko precizitāti.
Mums ir stingras iegādes vadlīnijas un tikai saikne ar cienījamiem mediju portāliem, akadēmiskām pētniecības iestādēm un, ja vien iespējams, medicīniski salīdzinošiem pārskatiem. Ņemiet vērā, ka iekavās ([1], [2] uc) esošie numuri ir klikšķi uz šīm studijām.
Ja uzskatāt, ka kāds no mūsu saturiem ir neprecīzs, novecojis vai citādi apšaubāms, lūdzu, atlasiet to un nospiediet Ctrl + Enter.
HPV 33 tips: simptomi, ārstēšana
Raksta medicīnas eksperts
Pēdējā pārskatīšana: 04.07.2025
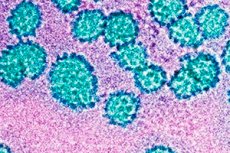
Mūsdienās medicīnā arvien biežāk parādās dažādas diagnozes un nesaprotami saīsinājumi, kas biedē tikai vienkāršu, neapgaismotu cilvēku. Spilgts piemērs ir diagnoze "HPV 33. tips". Kas ir šī dīvainā diagnoze? Aplūkosim visas detaļas sīkāk.
Kas tas ir?
Daudziem cilvēkiem ir jāveic laboratorijas testi. Saņemot rezultātus, asins analīzē var izlasīt tik biedējošu diagnozi. Pirmais, kas nāk prātā, ir kas tas ir? Izrādās, ka citiem vārdiem sakot, šo saīsinājumu var saukt par cilvēka papilomas vīrusu. Blakus tam ir norādīts celma kods - 33. Šis ir vīruss, kas diezgan bieži saglabājas kaukāziešu rases pārstāvjos.
Cilvēka papilomas vīruss (HPV) 33, kas pieder pie alfa-9 grupas, ir atbildīgs par aptuveni 5% no dzemdes kakla vēža gadījumiem visā pasaulē.[ 1 ],[ 2 ]
Struktūra 33. tipa HPV
Vīrusa struktūra ir ļoti specifiska. Pirmkārt, uzmanība tiek pievērsta faktam, ka vīrusa izmērs var svārstīties diezgan plašā diapazonā - no 100 līdz 200 nm. Membrānu veido divi slāņi. Pirmo slāni veido lipīdi, otro - glikoproteīnu komplekss. Komponenti ir savienoti viens ar otru ar nekovalentām saitēm.
Augsta riska HPV genotipi 33
Papilomas vīruss pieder pie Papillomaviridae dzimtas. Tā ir liela vīrusu grupa, kas izraisa audzējus.
Tika identificēti divdesmit astoņi HPV33 varianti, kas veidoja piecas filoģenētiskas grupas: iepriekš identificētās līnijas A1, A2 un B (apakšlīnijas) un jaunās līnijas A3 un C (apakšlīnijas).
HPV33 varianti ir klasificēti divās galvenajās līnijās — A un B. Līnija A ir tālāk sadalīta divās apakšlīnijās: A1, kas ietver prototipa secību [M12732.1 (Cole and Streeck, 1986) [ 3 ], un A2. Šī klasifikācija ir balstīta uz noteikšanu, ka galvenās varianta līnijas pilnā genoma secība atšķiras par aptuveni 1,0 % no citas tā paša HPV tipa varianta līnijas, un apakšlīnijas nosaka 0,5–0,9 % atšķirības (Chen et al., 2011). [ 4 ]
Apakšlīnijas A1 ir izplatītas visā pasaulē, lai gan relatīvais biežums atšķiras pa reģioniem. Apakšlīnijas A2 reti tika konstatētas Āfrikā un Dienvidamerikā, savukārt līnija B ir raksturīga Āfrikai. Apakšlīnijas C tika konstatētas tikai paraugos no Āfrikas, un apakšlīnijas A3 bija raksturīgas Āzijai/Okeānijai, ko apstiprina divi papildu ziņojumi no Ķīnas (Wu et al., 2009) [ 5 ] un Japānas [pamatojoties tikai uz E6 (Xin et al., 2001)] [ 6 ]. Tomēr, interpretējot šos rezultātus, jāņem vērā novērotā līniju A3 un C retums.
HPV DNS 33
Galvenā sastāvdaļa ir onkogēnu gēni, kas ietver olbaltumvielu komponentus. Tie nes informāciju, kas var izraisīt audzēja augšanu. HPV 33 DNS veido divas spirāles. Tas pastiprina vīrusa īpašības. Svarīga loma tiek piešķirta arī regulējošajiem šūnu gēniem, kas regulē galvenos šūnu procesus un transformācijas faktorus.
Dzīves cikls 33. tipa HPV
Vīrusa dzīve ir ciklisks process un notiek vairākos posmos.
Pirmajā posmā vīruss tiek absorbēts saimniekšūnu receptoros.Šis process ir iespējams, pateicoties glikoproteīnu klātbūtnei membrānas kompleksā un pašos virionos.
Otro posmu raksturo vīrusa aktīva iekļūšana tieši saimnieka šūnu struktūrā. Tas iedarbina galvenos vīrusa mijiedarbības mehānismus ar šūnu matricu. Pastāv dažādi mijiedarbības mehānismi.
Trešajā posmā vīruss pārvietojas pa šūnu, veidojot burbuļus, kuros tas ir īslaicīgi aizsargāts. Vīrusa transportēšanas pēdējais punkts ir ribosomu un endokrīnās restrikcijas receptora (ER) sasniegšana. Dažreiz vīrusu daļiņas un paši vīrusi migrē uz kodolu.
Ceturto posmu var raksturot kā viriona atdalīšanas procesu. Šī procesa būtība ir deproteinizācija un atbrīvošanās no superkapsīda un kapsīdām.
Piektajā posmā virions pilnībā izšķīst, un sākas vīrusu sintezēšanas process, kas pēc tam iznīcina šūnu un tiek izlaisti uz āru.
Sestajā posmā tiek salikts virions un izveidots nukleokapsīds. Tiek uzsākts vīrusu daļiņu pašsalikšanās process.
Septītajā posmā vīrusu daļiņas atstāj šūnu. Attiecīgi sākas infekcijas aktīvā stadija, tās progresēšana.
Pēc tam dzīves cikls atkārtojas, iesaistās jaunas šūnas, un attiecīgi slimība attīstās un progresē.
Pathogenesis
HPV galvenokārt tiek pārnests ādas kontakta ceļā. Epidemioloģiskie pētījumi skaidri norāda, ka dzimumorgānu HPV infekcijas un dzemdes kakla vēža iegūšanas risks ir saistīts ar seksuālo aktivitāti. HPV ir ļoti izturīgs pret karstumu un žāvēšanu, un var notikt arī aseksuāla transmisija, piemēram, ilgstošas saskares laikā ar piesārņotu koplietojamu apģērbu [ 7 ]. Cilvēkam ir lielāks risks iegūt HPV, ja viņam vai viņai jebkurā laikā ir bijuši vairāki seksuālie partneri vai ja viņš vai viņa ir partneris personai, kurai ir bijuši vairāki seksuālie partneri. Arī agrīna seksuālā aktivitāte pakļauj cilvēku paaugstinātam riskam, tāpat kā citu seksuāli transmisīvo slimību anamnēze, dzimumorgānu kārpas, patoloģiski Papa testi vai dzemdes kakla vai dzimumlocekļa vēzis pašam cilvēkam vai seksuālajam partnerim. Prezervatīvu lietošana var nepietiekami pasargāt cilvēkus no HPV iedarbības, jo HPV var pārnest, nonākot saskarē ar inficētiem kaunuma lūpu, sēklinieku vai anālo audu audiem, kurus neaizsargā prezervatīvs.
Papildus seksuālajai aktivitātei, vecums ir svarīgs HPV infekcijas riska faktors [ 8 ]. Visaugstākā metaplastiskā aktivitāte tiek novērota pubertātes un pirmās grūtniecības laikā, un tā samazinās pēc menopauzes. HPV infekcija visbiežāk ir seksuāli aktīvām jaunām sievietēm vecumā no 18 līdz 30 gadiem. Izplatība strauji samazinās pēc 30 gadu vecuma. Tomēr dzemdes kakla vēzis biežāk sastopams sievietēm, kas vecākas par 35 gadiem, kas liecina par inficēšanos jaunākā vecumā un lēnu vēža attīstību.
Primārā imūnreakcija uz HPV infekciju ir šūnu mediēta; tādēļ stāvokļi, kas pasliktina šūnu mediēto imunitāti, piemēram, nieru transplantācija vai cilvēku vīrusu slimības, palielina HPV iegūšanas un progresēšanas risku.[ 9 ],[ 10 ]
Dzemdes kakla šūnās ir pierādīta lokāla imūnsupresija, ko izraisa smēķēšana un cigarešu komponentu mutagēnā aktivitāte, un tā var veicināt HPV noturību vai ļaundabīgu transformāciju, līdzīgi kā novērots plaušās.[ 11 ],[ 12 ] Kopumā zināšanas par to, kā tiek pārnests HPV 33, var palīdzēt novērst infekciju.
Simptomi
Ir vairākas slimības formas. No tā ir atkarīgi simptomi. Slimības seksuālā tipa gadījumā tiek bojātas dzimumorgānu un reproduktīvās sistēmas gļotādas. Parādās sāpes, nieze, dedzināšana un kairinājums. Bieži vien simptomi atgādina piena sēnīti: parādās balti izdalījumi, dažreiz sieram līdzīgi. Kārpas, izaugumi un papilomas bieži parādās tieši uz maksts, dzemdes kakla kanāla un dzemdes gļotādas.
Ādas formā uz ādas var parādīties izaugumi un papilomas. Tie galvenokārt lokalizējas uz ādas augšējā slāņa - epidermas. Tie var būt plakani vai pacelti. Jāatzīmē arī, ka kārpas var diezgan ātri augt un vairoties. Tās var būt gan vienas, gan vairākas. Bieži vien kārpas ir vienīgā šīs slimības izpausmes forma.
Seksuāli transmisīva HPV infekcija izraisa vienu no trim iespējamiem iznākumiem.
- Pirmā ir anogenitālās kārpas (condyloma acuminatum), kas rodas uz dzimumorgāniem un anālās atveres vai ap tām gan vīriešiem, gan sievietēm.
- Otrais iznākums ir latenta jeb neaktīva infekcija, kuras gadījumā tikai retais zina, ka ir inficēts, jo pamanāmi simptomi parādās reti un inficētā zona citoloģiski paliek normāla. HPV DNS ir sastopama aptuveni 10 % sieviešu ar citoloģiski normālu dzemdes kakla epitēliju.
- Trešais iznākums ir aktīva infekcija, kas saistīta ar augsta riska HPV tipiem, kuros vīruss izraisa izmaiņas inficētajās šūnās, kas var izraisīt dzimumlocekļa, urīnizvadkanāla, maksts, vulvas vai dzemdes kakla intraepiteliālu neoplāziju. Augsta riska HPV tipi ietver tipus, kas saistīti ar dzemdes kakla vēzi, un tipus, kas definēti kā vidēja riska tipi, kas retāk sastopami vēža gadījumos. Šīs infekcijas var izraisīt dzemdes kakla vēzi. Prospektīvi pētījumi liecina, ka 15–28 % sieviešu, kurām bija pozitīva HPV DNS, 2 gadu laikā attīstījās SIL, salīdzinot ar tikai 1–3 % sieviešu, kurām bija negatīva HPV DNS.
Papilomas
Tas izskatās kā kārpa jeb neliels veidojums, kas paceļas uz kātiņa. Šo struktūru attēlo saistaudi. No augšas to klāj daudzslāņu epitēlijs. Tas var diezgan spēcīgi pacelties virs virsmas (uz kātiņa), uz kuras tas aug, un var būt arī plakans un izpleties horizontāli.
Augšanas temps ir diezgan zems, tas ir saistīts ar lēni augošiem audzējiem. Bīstamību rada audzēji, kas atrodas uz iekšējiem orgāniem: tie var tikt bojāti, izraisīt asiņošanu. Lokalizējoties iekšējo orgānu (balsenes, barības vada, zarnu) lūmenā, tie var augt un aizvērt lūmenu. Tas izraisa atbilstošas patoloģijas: nosmakšanu, obstrukciju. Šādi audzēji ir jānoņem. Galvenā papilomas ārstēšanas metode ir ķirurģiska, kas sastāv no tās izgriešanas.
HPV 33 vīriešiem
Diezgan bieži vīrieši ir šī vīrusa nesēji, taču slimība viņiem neizpaužas. Vīruss var saglabāties asinīs neaktīvā formā vai arī to vienkārši nomāc imūnsistēma. Taču, nonākot saskarē ar sievieti, viņa bieži inficējas, jo sievietēm ir daudz vājāka imunitāte, un tā neļauj viņām pilnībā pretoties infekcijai.
Galvenā izpausme ir papilomu veidošanās (vairākas, vienas). HPV 33 ārstēšanai vīriešiem tiek lietotas zāles, augu izcelsmes zāles un homeopātiskie preparāti.
HPV 33 sievietēm
Sievietes biežāk cieš no šī vīrusa. Šajā gadījumā dominē slimības dzimumorgānu forma. Visbiežāk tā izpaužas papilomu un kondilomu veidā, kas atrodas uz dzimumorgānu gļotādas. Bīstamība ir tāda, ka pastāv šo audzēju ļaundabīgas deģenerācijas iespēja, to pārveidošanās par ļaundabīgu audzēju. Jāatzīmē, ka bieži vien vienīgais veids, kā tos ārstēt, ir ķirurģiska izgriešana. Bet pēc tam ir nepieciešama papildu ārstēšana, kuras mērķis ir novērst recidīvu, novērst atkārtotus audzējus.
HPV 33 un mērena displāzija
To īpatnība ir tā, ka tie ir potenciāli onkogēni, tas ir, noteiktos apstākļos tie provocē ļaundabīgu audzēju attīstību: samazināta imunitāte, paaugstināta reaktivitāte un sensibilizācija, vājums, samazināta organisma izturība un rezistence, bioķīmiskā cikla traucējumi, normāls organisma strukturālais un funkcionālais stāvoklis, kā arī hormonālā nelīdzsvarotība. Šādos apstākļos attīstās papilomas, fibromas, miomas, fibromiomas, šķiedru veidojumi. Tā ir mērena displāzija, kas ir tieši saistīta ar HPV 33. Šo stāvokli var raksturot kā vēža priekšvēža stāvokli. Vienmēr pastāv potenciāls šo stāvokļu progresēšanas un pārejas uz ļaundabīgiem audzējiem - sarkomām, vēzi, leikēmiju - risks.
HPV 33 un grūtniecība
HPV 33 parādīšanās grūtniecības laikā ir slikta zīme, jo šis vīruss var izraisīt grūtniecības patoloģijas. Tās var būt spontāni aborti, spontānie aborti, priekšlaicīgas dzemdības vai nedzīvi dzimuši bērni. Bērniem bieži ir attīstības defekti: fiziskas deformācijas, dažādas garīgās un funkcionālās novirzes, kā arī garīga atpalicība (MR), garīgā atpalicība, runas defekti un emocionālā attīstība.
Taču šie ir ekstremāli gadījumi, kas rodas ar augstu vīrusu koncentrāciju, augstu vīrusu slodzi. Pretējā gadījumā, ārstējoties un pastāvīgi uzraugot ārstu, grūtniecība var noritēt normāli. Taču vienmēr pastāv risks saslimt ar uroģenitālā trakta infekciju, asiņošanu, kas īpaši pastiprinās dzemdību laikā. Pastāv paaugstināts bērna inficēšanās risks dzemdību laikā.
Diagnostika
Jums būs nepieciešams pieredzējis virusologs vai imunologs. Varat arī sazināties ar infekcijas slimību speciālistu, laboratorijas ārstu, bioķīmiķi, bakteriologu. Ja klīnikā nav šādu speciālistu, jums jāsazinās ar attiecīgajā jomā norīkoto terapeitu, un viņš jūs nosūtīs pie pareizā speciālista vai vienkārši nozīmēs nepieciešamos izmeklējumus. Galvenā diagnozes apstiprināšanas metode ir tieša vīrusa klātbūtnes apstiprināšana asinīs, ko var panākt tikai veicot atbilstošus testus. Tiek izmantotas laboratorijas metodes (tās ir vienīgās efektīvās un uzticamās pētījumu metodes).
Vairumā gadījumu pētījuma materiāls ir asinis. Tiek izrakstītas viroloģiskās un seroloģiskās pētījumu metodes, kas ļauj noteikt pašu vīrusu asinīs, tā dzīvības aktivācijas produktos vai DNS (tā fragmentos). Laboratorijā tiek izmantotas dažādas analīzes metodes. Bet vīrusa noteikšanai ir vērts izmantot PCR metodi jeb DNS sekvencēšanu, ar kuras palīdzību asinīs tiek atklāti paši vīrusi, nevis antivielas kā imūnsistēmas reakcija uz vīrusa ieviešanu.
Tipspecifiskas PCR analīzes ir balstītas uz secības variācijām, kas atrodas HPV apakštipu E6 un E7 gēnos. Četrpadsmit tipspecifiskas PCR analīzes augsta riska HPV tipiem (HPV-16, -18, -31, -33, -35, -39, -45, -51, -52, -56, -58, -59, -66 un -68) ir vērstas uz aptuveni 100 bp E7 ORF ietvaros. [ 13 ]
Genomu veido vairāk nekā 100 000 nukleotīdu, 9 gēni. Uz iekšējās virsmas atrodas matricas karkass. To veido proteīni p17/18. Genomu veido 3 strukturālie gēni un 6 regulējošie gēni. Jāatzīmē arī, ka vīruss ir diezgan mainīgs, īpaši salīdzinot ar citiem vīrusiem. Vairāki pētnieki joprojām strādā pie HPV 33. tipa DNS atšifrēšanas.
ELISA (enzīmu imūnsorbcijas testa) metode nav informatīva, jo tā reaģē uz antigēna-antivielu kompleksa daudzumu. Turklāt antivielas pēc vienas saslimšanas saglabājas visu mūžu. Tāpēc nav iespējams izdarīt secinājumus par vīrusinfekcijas stadiju un aktivitātes pakāpi organismā.
Svarīga ir arī ārsta apskate. Viņš veiks visaptverošu pārbaudi un noteiks diagnozi. Vizuālas pārbaudes laikā ārsts jau varēs aizdomas par HPV 33. tipa klātbūtni, jo tas izpaužas ar specifiskām pazīmēm. Bet, lai galīgi apstiprinātu slimību, ir svarīgi ne tikai to diagnosticēt, bet arī veikt diferenciāldiagnozi. Tas nozīmē, ka simptomi ir jādiferencē no citiem līdzīgiem gadījumiem un līdzīgām izpausmēm.
Papildu metodes var ietvert mikroskopisku izmeklēšanu, skrāpēšanu. Atkarībā no patoloģijas smaguma pakāpes var būt nepieciešama imunogramma, klīniskās un bioķīmiskās asins un urīna analīzes, disbakteriozes testi.
Mikroskopija palīdzēs identificēt pašu vīrusu vai tā atkritumproduktus uztriepē, izpētīt tā pazīmes un specifiskās īpašības mikroskopā. Pamatojoties uz šiem datiem, ir iespējams noteikt patogēna skaidru sistemātisku pozīciju līdz pat sugai un ģintij. Jo precīzāk šāda identifikācija tiek veikta, jo precīzāk un efektīvāk būs iespējams izvēlēties ārstēšanu. Ir svarīgi arī iegūt kvantitatīvus rādītājus, jo turpmākās ārstēšanas plāns un tās efektivitāte ir atkarīga no vīrusa daudzuma asinīs (vīrusu slodzes).
Galvenā augsta riska HPV noteikšanas metode joprojām ir Pap uztriepe (PAP). Šis tests tika nosaukts patologa Džordža Papanikolau vārdā, kurš ieviesa šo testu 1949. gadā, pirms bija zināms dzemdes kakla vēža cēlonis. Kopš ieviešanas Pap uztriepe ir palīdzējusi samazināt dzemdes kakla vēža saslimstību un mirstību par aptuveni pusi līdz divām trešdaļām. [ 14 ] Pap uztriepe ir skrīninga rīks, kas meklē izmaiņas dzemdes kakla transformācijas zonas šūnās. Bieži vien šīs izmaiņas izraisa HPV.
HPV norma 33
No medicīniskā un bioloģiskā viedokļa par normu tiek uzskatīta pilnīga vīrusu neesamība asinīs. Taču tas ir ideāls gadījums, kas mūsdienu dzīves apstākļos ir ārkārtīgi reti sastopams. Tāpēc pastāv noteiktas HPV 33 nosacītas normas organismā. Taču tās dažādās valstīs ievērojami atšķiras. Ir tikai dažas valstis, kurās vīrusa absolūta neesamība asinīs tiek uzskatīta par normu.
Ārstēšana
Ārstēšana galvenokārt sastāv no neoplazmu ķirurģiskas izgriešanas. Mūsdienās papildus tradicionālajai ķirurģijai ir liels skaits papilomu noņemšanas metožu. Tādējādi visefektīvākās metodes ir lāzera noņemšana, krioterapija, radioviļņu un radiofrekvences, elektrokoagulācija, termiskā, elektrotermiskā papilomu noņemšana. Pastāv arī papilomu noņemšana, izmantojot ķīmiskas vielas.
Lielākā daļa HPV izraisīto izmaiņu dzemdes kakla šūnās ir pārejošas, un 90 % no tām spontāni izzūd 12–36 mēnešu laikā, imūnsistēmai iznīcinot vīrusu.[ 15 ]
Tradicionāli ir izmantota pretvīrusu terapija. Piemēram, tradicionālās zāles ir inoziplekss, interferons, amiksīns, cikloferons, podofilīns. Podofilīns, citotoksisks līdzeklis, kas aptur mitozi metafāzē (lieto arī dzimumorgānu kārpu ārstēšanai), kombinācijā ar vidarabīnu, DNS polimerāzes inhibitoru, kas nomāc HPV gēnu ekspresiju un šūnu augšanu dzemdes kakla vēža šūnu līnijās. [ 16 ]
Klīniskajos un in vitro pētījumos IFN un intravaginālam 5-fluoruracilam ir novērota mainīga atbildes reakcija. IFN-α ir apstiprināts dzimumorgānu kārpu ārstēšanai. IFN-α, IFN-β un IFN-γ ietekme ir pētīta vairākās cilvēka karcinomas šūnu līnijās.[ 17 ]
Ir svarīgi veikt imunomodulējošu terapiju, kuras mērķis ir normalizēt imunitātes stāvokli. Parasti ir nepieciešama imunostimulējoša terapija, kuras pamatā ir imunitātes paaugstināšana. Rezultātā imūnsistēma patstāvīgi pretojas infekcijai, palielinās tās rezistence un izturība, un vīruss tiek nomākts.
Tradicionālā ārstēšana tiek izmantota profilaksei, pēcoperācijas atveseļošanai vai vienkārši kā efektīvs līdzeklis mikrofloras skaita un vīrusu slodzes samazināšanai. Tā var būt zāļu terapija, dažādi fizioterapeitiskie līdzekļi, tradicionālā medicīna, homeopātija un fitoterapija. Tiek veiktas arī profilaktiskas pretvīrusu vakcinācijas, kas palīdz novērst šūnu ļaundabīgu deģenerāciju. Veidojoties kondilomām un papilomām, bieži tiek izmantota to piededzināšana un dedzināšana.
Ko darīt, ja tiek atklāts HPV 33?
Pirmkārt, jums jāapmeklē ārsts, kurš izvēlēsies atbilstošu ārstēšanu. Jo ātrāk ārstēšana tiks uzsākta, jo efektīvāka tā būs. Ārsts, pamatojoties uz laboratorijas un instrumentālo pētījumu rezultātiem, pateiks, kā rīkoties. Ja tiek atklāts HPV 33, var būt nepieciešama medikamentoza vai ķirurģiska ārstēšana (papilomas izgriešana). Tiek izmantota arī pretvīrusu, imunostimulējoša terapija.
Vai ir iespējams izārstēt HPV 33?
Šī patoloģija labi reaģē uz ārstēšanu, ja imūnsistēma ir normāla. Tātad, ja imūnsistēma ir zema, var novērot dažādus saasinājumus, slimības un recidīvus. Bīstamība ir tāda, ka vīruss ir potenciāli onkogēns. Ja imūnsistēma ir normāla, vīruss var vienkārši saglabāties asinīs, neizraisot infekcijas saasināšanos.
Tādējādi, atbildot uz jautājumu: "Vai ir iespējams izārstēt HPV 33", nav iespējams sniegt nepārprotamu atbildi. Tāpēc ir svarīgi uzturēt imunitāti normālā līmenī. Izvairieties no pārslodzes, stresa. Veicot pretvīrusu terapiju, stimulējot imūnsistēmu, vitamīnu terapiju, vīrusu ir iespējams pārnest neaktīvā stāvoklī. Tad tas saglabāsies asinīs, neizraisot akūtu slimību. Taču pilnībā izvadīt vīrusu no asinīm ir gandrīz neiespējami, cilvēks paliek vīrusa nesējs un var inficēt citus.
Profilakse 33. tipa HPV
Profilakses pamatā ir higiēnas noteikumu ievērošana, atbilstoša dzimumdzīve (pastāvīga partnera klātbūtne, aizsardzības līdzekļu lietošana, nonākot saskarē ar pagaidu partneriem, profilaktiska ārstēšana, ja seksuālajam partnerim ir infekcija). Šie ir galvenie un pamata profilakses pasākumi. Svarīgi ir arī uzturēt normālu imūnsistēmu – periodiski konsultēties ar imunologu, veikt vīrusu, latentu infekciju testus, lietot vitamīnu kursus un, ja nepieciešams, imūnstimulējošus līdzekļus.
Ir svarīgi ēst pareizi, iekļaut uzturā nepieciešamo vitamīnu un minerālvielu daudzumu, regulāri veikt profilaktiskās pārbaudes un, ja nepieciešams, savlaicīgi ārstēties. Īpaši svarīgi ir uzturēt augstu imunitātes līmeni, jo slimības attīstība ir iespējama tikai ar samazinātu imunitāti un traucētu mikrofloru.
Galvenās pieejas HPV infekcijas profilaksei ietver gan riska samazināšanu, gan HPV vakcīnu izstrādi. Lateksa prezervatīvu un spermicīdu lietošana var samazināt HPV infekcijas risku. Tomēr prezervatīvi nav pilnībā uzticami, jo HPV var tikt pārnests, nonākot saskarē ar citām ķermeņa daļām, piemēram, kaunuma lūpām, sēklinieku maisiņu vai anālo atveri, kuras prezervatīvs neaizsargā.
Izmantojot apakšvienību vakcīnu, kas sastāvēja no VLP, kas ģenerēts no HPV-16 celma 114K visa L1 galvenā kapsīda proteīna [ 18 ], tika veikts I fāzes, dubultmaskēts, randomizēts, placebo kontrolēts drošības un imunogenitātes pētījums. Vakcīna tika iegūta, ievietojot L1 kapsīda gēnu bakulovīrusa vektorā. Pēc tam gēns tika ekspresēts transfektētās Sf9 kukaiņu šūnās. Optimāla HPV-16 L1 VLP vakcīnas deva 50 μg tika ievadīta, injicējot deltveida muskulī 0, 1 un 4 mēnešos. Vakcīna ģenerēja augstus tipam specifisku neitralizējošo antivielu titrus bez adjuvanta un bija labi panesama.
Sākot ar 2017. gadu, Gardasil 9® ir vienīgā HPV vakcīna, kas pieejama Amerikas Savienotajās Valstīs. Citas HPV vakcīnas ir pieejamas ārpus Amerikas Savienotajām Valstīm. Gardasil 9 palīdz novērst inficēšanos ar 4 HPV tipiem (16, 18, 6 un 11) un 5 citiem augsta riska tipiem: 31, 33, 45, 52 un 58. Kopā šie tipi izraisa aptuveni 90% dzemdes kakla vēža gadījumu.
Amerikas vēža biedrības ieteikumi par HPV vakcīnas lietošanu.
- Rutīnas HPV vakcinācija meitenēm un zēniem jāsāk 11–12 gadu vecumā. Vakcinācijas sēriju var sākt jau 9 gadu vecumā.
- HPV vakcinācija ir ieteicama arī sievietēm vecumā no 13 līdz 26 gadiem un vīriešiem vecumā no 13 līdz 21 gadam, kuri vēl nav sākuši vakcinācijas sēriju vai ir sākuši, bet nav pabeiguši sēriju. Vakcinēties var arī vīrieši vecumā no 22 līdz 26 gadiem.
- HPV vakcinācija ir ieteicama arī 26 gadu vecumā vīriešiem, kuriem ir dzimumattiecības ar vīriešiem, un cilvēkiem ar novājinātu imūnsistēmu (tostarp cilvēkiem ar HIV infekciju), ja viņi iepriekš nav vakcinēti.
- Cilvēkiem vecumā no 22 līdz 26 gadiem, kuri vēl nav sākuši vakcināciju vai ir sākuši, bet nav pabeiguši vakcinācijas kursu, ir svarīgi zināt, ka vakcinācija vecākā vecumā ir mazāk efektīva vēža riska mazināšanā.
Prognoze
Vairumā gadījumu ar pareizu un savlaicīgu ārstēšanu prognoze būs labvēlīga. HPV 33. tipu ir diezgan viegli izvadīt, galvenais ir saglabāt normālu imunitāti, ievērot visus ārsta ieteikumus. Ja parādās papilomas, var būt nepieciešama to ķirurģiska noņemšana (izgriešana). Šī ir ātra un nesāpīga procedūra, kas praktiski neprasa atveseļošanos. Svarīga loma ir pretvīrusu ārstēšanai. Ja to neārstē, var rasties komplikācijas. Visbīstamākais ir ļaundabīgu audzēju attīstība.

